STUDIEN
Liebe PatientInnen, liebe Studienteams,
hier finden Sie einen kurzen Überblick unserer aktueller Studien.
Für weitergehende Informationen oder bei Interesse an einer Teilnehme, kontaktieren Sie uns bitte hier.
Rekrutierende Studien
NeoNeoAdjuvant Dynamic marker - Adjusted Personalized Therapy comparing sacituzumab govitecan versus
sacituzumab govitecan+pembrolizumab in low-risk, triplenegative early breast cancer
Deutsche Übersetzung:
NeoAdjuvante, an Dynamischen Markern Adjustierte, Personalisierte Therapie mit Sacituzumab Govitecan im Vergleich zu Sacituzumab Govitecan + Pembrolizumab in frühem, triple-negativem Brustkrebs mit niedrigem
Rezidivrisiko
1. Patientenklientel:
- Jedes Geschlecht
- Prä- oder postmenopausal
- mit invasivem, unbehandeltem triple negativem Brustkrebs
- Niedriges bis mittleres klinisches Rezidivrisiko (Stadium I und II)
2. Studiendesign:
- Multizentrisch
- Interventionell, Phase II
- Zweiarmig randomisiert
- Prospektiv
- offen, kontrolliert

3. Studienziele:
Ziel der ADAPT-TN-III Studie ist es, eine gut verträgliche und hochwirksame deeskalierte Therapie bei frühem triple negativen Brustkrebs zu untersuchen, mit dem Ziel, länger dauernde und toxischere Behandlungen zu vermeiden. Es wird untersucht, ob die Kombinationstherapie von Sacituzumab Govitecan + Pembrolizumab eine höhere Rate an pathologischer Komplettremission erreicht als die Therapie mit Sacituzumab Govitecan alleine. Weiterhin wird das 3-Jahres-Überleben in beiden Armen im Vergleich zu historischen Kontrollen untersucht
NeoAdjuvant Dynamic marker - Adjusted Personalized Therapy comparing trastuzumab-deruxtecan versus pacli-/docetaxel+carboplatin+trastuzumab +pertuzumab in HER2+ early breast cancer
Deutsche Übersetzung:
Neoadjuvante, an dynamischen Makern adjustierte, personalisierte Behandlung von frühem, HER2-positivem Brustkrebs mit Trastuzumab-Deruxtecan im Vergleich zu Pacli-/Docetaxel+Carboplatin+Trastuzumab +Pertuzumab
1. Patientenklientel:
- Weibliche Patienten
- Prä- oder postmenopausal
- mit invasivem, unbehandeltem HER2+ Brustkrebs maximal 6 Wochen vor Registrierung diagnostiziert
- Niedriges, mittleres oder hohes klinisches Rezidivrisiko
2. Studiendesign:
- Multizentrisch
- Interventionell, Phase II
- Zweiarmig randomisiert
- Prospektiv
- offen, kontrolliert

3. Studienziele:
ADAPT-HER2-IV ist als Überlegenheitsstudie geplant, um höhere pCR-Raten (pathologische Komlettremision) in beiden klinisch relevanten Untergruppen von HER2+frühem Brustkrebs mit niedrigem bis mittlerem Risiko nachzuweisen. Darüber hinaus zielt es darauf ab, ein hervorragendes Überleben bei mit T-DXd behandelten Patienten zu untersuchen und damit zu zeigen, ob eine Optimierung/De-Eskalation der Therapie des frühen HER2+ Mammakarzinoms mit diesem Ansatz möglich ist.
PROOFS-Registry
Real world data and long-term follow-up of female patients with luminal early breast cancer with intermediate to high clinical risk for recurrence and (ultra)low or increased genomic recurrence-risk measured by MammaPrint®, who are considered for therapy de-escalation and treated by standard-of-care endocrine treatment (with/without ovarian function suppression) or standard-of-care chemotherapy followed by endocrine treatment.
Deutsche Übersetzung:
Daten aus der klinischen Praxis und Langzeitnachsorge weiblicher Patientinnen mit luminalem Brustkrebs im Frühstadium, der ein mittleres bis hohes klinisches und (ultra-)niedriges oder erhöhtes genomisches Rezidivrisiko (bestimmt mittels MammaPrint®) aufweist, die Kandidatinnen für eine de-eskalierte Behandlung sind und mit endokriner Therapie (mit oder ohne Unterdrückung der Ovarialfunktion (OFS)) oder Standard-Chemotherapie, gefolgt von einer endokrinen Therapie, behandelt werden.
1. Patientenklientel:
- Patientinnen mit frühem Mammakarzinom
- HR-positiv
- HER2-negativ
- Mittleres oder hohes klinisches Rezidivrisiko
- Prä-, peri- oder postmenopausal
- Niedriges oder erhöhtes genomisches Rezidivrisiko bestimmt durch MammaPrint®
2. Studiendesign:
Nicht-interventionelle Studie zur Evaluation des Fernrezidiv-freien Überlebens bei allen Patientinnen, die mit (intensivierter) endokriner Therapie allein (ohne Chemotherapie) - und mit ovarieller Suppression in Fällen mit erhöhtem klinischem Risiko gemäß den aktuellen AGO-Empfehlungen - behandelt wurden.
- Multizentrisch
- nicht-interventionell
- Prospektiv

3. Studienziele:
Die PROOFS-Registry-Studie zielt auf die Beantwortung folgender Fragen ab:
- Welches ist die optimale endokrine Therapie für prä-, peri- und postmenopausale Patientinnen?
- Welchen Einfluss hat die ovarielle Suppression auf das Langzeit-Überleben und die Langzeit-Lebensqualität?
- Lässt sich ein möglicher Chemotherapie-Nutzen auf die Chemotherapie-induzierte Amenorrhoe zurück führen?
- Welchen prognostischen Stellenwert haben klinische und genomische Risikofaktoren?
- Wie ist die Therapieadhärenz?
Studien im Follow up

A randomized, controlled, open-label, phase-III trial on Adjuvant Dynamic marker - Adjusted Personalized Therapy comparing abemaciclib combined with standard adjuvant endocrine therapy versus standard adjuvant endocrine therapy in (clinical or genomic) intermediate to high risk, HR+/HER2- early breast cancer
Deutsche Übersetzung:
Eine randomisierte, kontrollierte, offene, adjuvante, an Dynamischen Markern adjustierte, personalisierte Therapiestudie der Phase-III zum Vergleich der Therapie von Abemaciclib plus endokriner Standardtherapie gegenüber alleiniger adjuvanter endokriner Standardtherapie bei Hormonrezeptor-positivem, HER2-Rezeptor negativem Brustkrebs im Frühstadium mit klinisch oder genomisch mittleren bis hohem Risiko für ein Spätrezidiv
1. Patientenklientel:
- Patientinnen mit frühem Mammakarzinom (nicht metastasiert)
- HR-positiv
- HER2-negativ
- Primärdiagnose vor nicht mehr als 6 Jahren
- Einschluss in die Studie ab Primärdiagnose möglich, Randomisierung erst nach abgeschlossener lokaler Behandlung des Brustkrebses
- Geplante oder laufende endokrine Therapie
- Bekanntes hohes klinisches oder hohes genomisches Risiko oder mittleres klinisches Risiko bei unbekanntem genomischem Risiko
2. Studiendesign:
Dies ist eine multizentrische, interventionelle, prospektive, zweiarmige, randomisierte, offene, kontrollierte, adjuvante Phase-III-Studie zur Untersuchung der Wirksamkeit und Sicherheit einer Behandlung mit Abemaciclib kombiniert mit endokriner Therapie (ET) im Vergleich zur endokrinen Standardtherapie bei Patientinnen mit Brustkrebs im Frühstadium (EBC) mit dem molekularen Subtyp HR+/HER2-
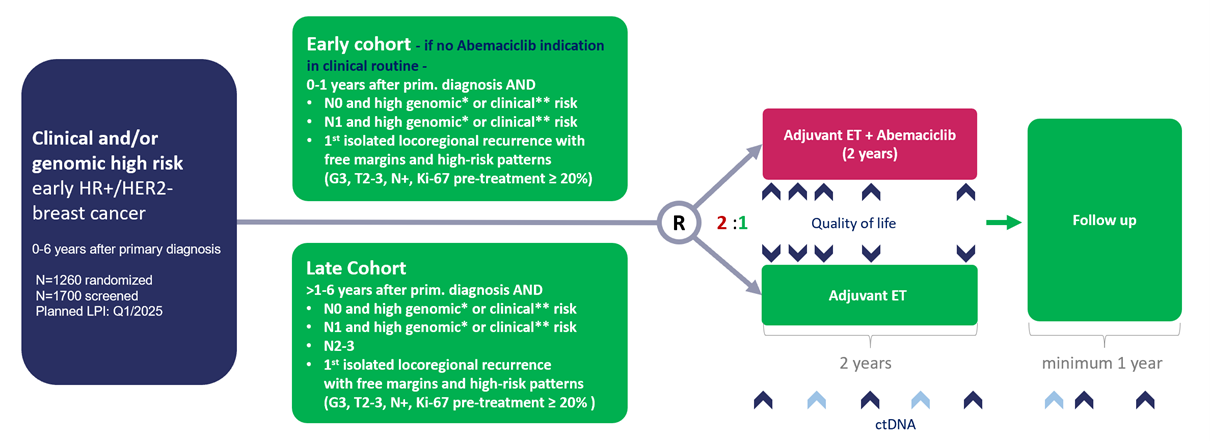
3. Studienziele:
Das Ziel dieser ADAPTlate Phase-III-Studie ist es, herauszufinden ob der "späte" Einsatz von Abemaciclib in der adjuvanten Therapie in der Lage ist, das Outcome beim frühen Brustkrebs für Patientinnen mit hohem Rezidivrisko zu verbessern.

Adjuvant Dynamic marker - Adjusted Personalized Therapy comparing endocrine therapy plus ribociclib versus chemotherapy in intermediate risk, HR+/HER2- early breast cancer
Deutsche Übersetzung:
Adjuvante, auf dynamische Marker adjustierte, personalisierte Therapie zum Vergleich einer endokrinen Behandlung plus Ribociclib mit Chemotherapie bei Hormonrezeptor-positivem, HER2-Rezeptor negativem, mittleres Risiko aufweisendem, frühen Brustkrebs
1. Patientenklientel:
- Patientinnen mit frühem Mammakarzinom
- HR-positiv
- HER2-negativ
- Intermediäres Reszidivrisiko
- Prä- oder postmenopausal
- Adjuvantes oder neoadjuvantes Setting
2. Studiendesign:
Phase-III Studie zur Evaluation der Wirksamkeit und Sicherheit einer Behandlung mit Ribociclib, kombiniert mit endokriner Therapie (ET),
im Vergleich zur Standard-Chemotherapie
- Multizentrisch
- Interventionell
- Prospektiv
- 2-armig
- Randomisiert
- Offen
- Kontrolliert

3. Studienziele:
Das Ziel dieser ADAPTcycle Phase-III-Studie ist es herauszufinden, ob die während der Screening Phase identifizierte Patientengruppe mit intermediärem Risiko für ein Rezidiv, einen Zusatznutzen von einer Behandlung mit Ribociclib in Kombination mit ET hat, verglichen mit einer Standard-Chemotherapie (gefolgt von adjuvanter ET).
A prospective, multicenter, open label, neoadjuvant phase II single arm study with pembrolizumab in combination with dual anti-HER2 blockade with trastuzumab and pertuzumab in early breast cancer patients with molecular HER2-enriched intrinsic subtype
Deutsche Übersetzung:
Eine prospektive, multizentrische, offene, neoadjuvante, einarmige Phase II Studie mit Pembrolizumab in Kombination mit einer dualen Anti-HER2-Blockade mit Trastuzumab und Pertuzumab bei Patientinnen im Frühstadium von Brustkrebs mit molekularem HER2-angereichertem intrinsischem Subtyp
1. Patientenklientel:
- Patientinnen mit frühem Mammakazinom
- HR-positiv/-negativ
- HER2 positiv
- Prä- und postmenopausal
- Neoadjuvantes Setting
2. Studiendesign:
Dies ist eine multizentrische, interventionelle, prospektive, einarmige, offene, neoadjuvante Phase-II-Studie zur Evaluierung der pathologischen Komplettremissions-(pCR)-Rate, welche durch Pembrolizumab in Kombination mit der dualen Anti-HER2-Blockade, bestehend aus Trastuzumab-Biosimilar (Trazimera®) und Pertuzumab, induziert wird, bei Brustkrebspatientinnen im Frühstadium, mit molekularem HER2-angereicherten intrinsischen Subtyp, welcher mittels PAM50 Testung bestätigt wurde.

3. Studienziele:
Das primäre Ziel dieser Studie ist die Evaluierung der pCR-Rate der Kombinationstherapie, bestehend aus dem PD-1-Inhibitor Pembrolizumab in Kombination mit der dualen Anti-HER2-Blockade Trastuzumab-Biosimilar und Pertuzumab bei Patientinnen mit HER2-angereichertem Brustkrebs im Frühstadium, welcher durch den PAM50-Test bestätigt wurde.
Long term follow up registry for outcome evaluation in HR-positive/HER2 negative early breast cancer patients treated within the prospective PlanB study and relapse free after 5 years of endocrine therapy
Deutsche Übersetzung:
Langzeit-Follow up-Register zur Beobachtung des Überlebens von Patienten, die an einem HR positiven / HER2 negativen, primären Brustkrebs erkrankt sind, im Rahmen der prospektiven PlanB-Studie behandelt wurden und am Ende der Hormontherapie nach 5 Jahren rezidivfrei waren
1. Patientenklientel:
- HR+/HER2- Brustkrebs
- Teilnahme und Behandlung in der PlanB-Studie
- Vollständige Teilnahme an der PlanB-Studie inklusive des 5-Jahres Follow Up nach initialer Diagnose
- Rezidivfrei bis zu 5 Jahre nach der initialen Diagnose
2. Studiendesign:
Dies ist ein offenes, prospektives, multi-zentrisches, beobachtendesl, nicht-interventionelles Register zu Patienten, die an der PlanB Studie teilgenommen haben.

3. Studienziele:
Die PlanB-Studie endete im Mai 2017 und befindet sich derzeit in der statistischen Auswertung. Das Register ist dafür konzipiert die Daten früherer Teilnehmerinnen der PlanB-Studie bezüglich ihres Gesamtüberlebens für weitere 5 Jahre nach Abschluss der Studie (bzw. 10 Jahre nach der initialen Diagnose), ihrer rezidivfreien und (invasiv-) krankheitsfreien Zeit, sowie ihrer zusätzlichen Krebstherapien mit einem speziellen Fokus auf die anti-hormonelle Therapie (wenn angewendet), zu erfassen.

Adjuvant Dynamic marker-Adjusted Personalized Therapy trial optimizing risk assessment and therapy response prediction in early breast cancer
Deutsche Übersetzung:
Adjuvante, an dynamischen Tumormarkern orientierte, personalisierte Therapie bei Brustkrebs im frühen Stadium, bei der die Risikoeinschätzung und die Vorhersage des Therapieansprechens optimiert wird
1. Patientenklientel:
Patientinnen mit frühem Brustkrebs in verschiedenen Subgruppen (jeweils eigene Substudie):
1) HR+/HER2-
2) HR+/HER2+ (triple positive)
3) HR-/HER2+
4) HR-/HER2- (triple negative)
5) Elderly
Die Substudien 2) bis 5) sind bereits abgeschlossen, inklusive Follow-Up.
Die HR+/HER 2- Substudie befindet sich bezüglich der Chemotherapie-Fragestellung aktuell im Follow-Up
2. Studiendesign:
Prospektive, multizentrische, randomisierte Phase III Studie

3. Studienziele:
In der ADAPT Studie werden sowohl die persönlichen Risikofaktoren als auch das vorhergesagte Therapieansprechen berücksichtigt, um jeder Patientin eine individuelle, optimierte Therapie anbieten zu können. Ziele der Studie sind die Untersuchung der Wirksamkeit und der Verträglichkeit der verabreichten Therapien sowie die Verteilung der Risikoprofile.
Weitere Informationen & Erklärungen

A randomized, controlled, open-label, phase-III trial on Adjuvant Dynamic marker - Adjusted Personalized Therapy comparing abemaciclib combined with standard adjuvant endocrine therapy versus standard adjuvant endocrine therapy in (clinical or genomic) high risk, HR+/HER2- early breast cancer
Deutsche Übersetzung:
Eine randomisierte, kontrollierte, offene, adjuvante, an Dynamischen Markern adjustierte, personalisierte Therapiestudie der Phase-III zum Vergleich der Therapie von Abemaciclib plus endokriner Standardtherapie gegenüber alleiniger adjuvanter endokriner Standardtherapie bei Hormonrezeptor-positivem, HER2-Rezeptor negativem Brustkrebs im Frühstadium mit klinisch oder genomisch hohem Risiko für ein Spätrezidiv
1. Patientenklientel:
- Patientinnen mit frühem Mammakarzinom (nicht metastasiert)
- HR-positiv
- HER2-negativ
- Primärdiagnose vor nicht mehr als 6 Jahren
- Einschluss in die Studie ab Primärdiagnose möglich, Randomisierung erst nach abgeschlossener lokaler Behandlung des Brustkrebses
- Geplante oder laufende endokrine Therapie
- Bekanntes hohes klinisches oder hohes genomisches Risiko oder mittleres klinisches Risiko bei unbekanntem genomischem Risiko
2. Studiendesign:
Dies ist eine multizentrische, interventionelle, prospektive, zweiarmige, randomisierte, offene, kontrollierte, adjuvante Phase-III-Studie zur Untersuchung der Wirksamkeit und Sicherheit einer Behandlung mit Abemaciclib kombiniert mit endokriner Therapie (ET) im Vergleich zur endokrinen Standardtherapie bei Patientinnen mit Brustkrebs im Frühstadium (EBC) mit dem molekularen Subtyp HR+/HER2-